Технология минеральных солей (удоБрений, пестицидов, промышленных солей, окислов и кислот)
ЦИАНИСТЫЕ СОЕДИНЕНИЯ
К цианистым соединениям относятся вещества, содержащие одновалентную группу циана CN и его производные В свободном виде может быть выделен газообразный циан (С1Ч)Ж, представляющий собой в большинстве случаев дициан (CN)2, находящийся в равновесии 2 при высоких температурах с CN. Дициан является одним из наиболее реакционноспособных газов. Он легко реагирует с металлами и окислами металлов (образуя цианиды и цианамиды), с галогенами и различными органическими веществами. Из неорганических соединений циана наибольшее техническое значение имеют: синильная кислота HCN и цианиды калия, натрия и другие, цианамид CN-NH2 и кальцийцианамид, а также ферро - и феррицианиды калия и железа.
ФИЗИКО-ХИМИЧЕСКИЕ СВОЙСТВА
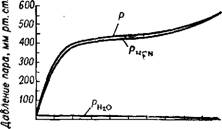
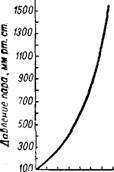
Цианистоводородная или синильная кислота HCN — бесцветная жидкость с запахом горького миндаля. Она кипит при 25,65°, замерзает при —13,4°. Плотность жидкости при 18° 0,6967 г/см3. С. водой смешивается во всех отношениях. На рис. 451 показана кривая давления пара чистой синильной кислоты, а на рис. 452 давление пара ее водных растворов при 18°. Пары HCN горят голубо - ватым пламенем.
|
Hcoonh4 |
Синильная кислота и ее водные растворы устойчивы лишь в присутствии стабилизаторов — небольших количеств свободных минеральных кислот. Без стабилизаторов, и особенно в присутствии следов щелочей, синильная кислота постепенно темнеет, что связано с образованием продуктов ее полимеризации. При кипячении водных растворов (а также в щелочной среде) частично идет гидролиз HCN с образованием формиата аммония3:
Hcn + 2н20
Кислотные свойства синильной кислоты выражены весьма слабо, и она легко вытесняется из своих солей другими кислотами, в том числе угольной. Поэтому под действием атмосферного воздуха, содержащего двуокись углерода, из цианидов выделяются пары HCN.
Цианистый натрий NaCN образует бесцветные кристаллы кубической формы. Кристаллизуется с двумя и с одной молекулой
|
-20 0 20 40 Температура, °С |
|
Рис. 451. Зависимость давления пара синильНой кислоты от температуры. |
Воды, а выше 34,7° — в безводной форме. Температура плавления безводной соли 563,7°. Насыщенный водный раствор содержит при 0° 43,4%. при 34,7° 82,0% NaCN.
|
0 10 20 30 40 50 60 70 80 90 100 HCN В жидкости, мол. % Рис. 452. Давление паров над водными Растворами синильной кислоты при 18": Р — общее давление паров, рт.„., — давление HHa - HUIN Иистого водорода, PJj^Q —давление водяного пара. |
Цианистый калий KCN кристаллизуется в безводной форме, образуя бесцветные октаэдрические кристаллы. Плавится при 634,5°. Расплывается на воздухе.
Цианиды натрия и калия достаточно устойчивы при нагревании вплоть до 800°. В смеси с хлоридами щелочноземельных металлов В расплавленном состоянии они превращаются в цианамидные соли 4:
2NaCN + ВаС12 = 2NaCl + Ba(CN)2
Ba(CN)2 = BaCN2 + C BaCN2 + 2NaCl = Na2CN2 + BaCl2
Цианистый кальций Ca(CN)2 выделяется из водных растворов в виде кристаллов кубической формы. Раствор соли и твердая соль во влажном воздухе легко теряют синильную кислоту, переходя при этом в основные соединения.
Синильная кислота (как жидкая, так и парообразная) и ее соли чрезвычайно ядовиты. Для человека смертельной дозой является 0,05 г HCN.
Цианамид кальция CaCN2— кальциевая соль цианамида Н2СКТ2 представляет собой бесцветные кристаллы с плотностью 2,3 г/см3. Технический продукт имеет темно-серый цвет вследствие присутствия в нем 10—15% углерода. Растворимость CaCN2 в 100 г воды при 25° равна 2,5 г. В водном растворе CaCN2 гидролизуется:
2CaCN2 + 2Н20 = Ca(HCN2)2 + Са(ОН)2
С течением времени кисл-ая соль цианамида кальция разлагается с образованием карбамида CO(NH2)2, дицианамида (H2CN2b и других продуктов. На воздухе под влиянием двуокиси углерода и влаги вначале образуется соединение CaCN2-C02-5H20, которое затем гидролизуется.
При взаимодействии CaCN2 с С02 в воде образуется цианамид, который при нагревании раствора до 80—90° полимеризуется в ди - цианамид5. Чистый CaCN2 устойчив в атмосфере азота до 1200°, плавится при 1340°. При нагревании диссоциирует в твердом состоянии. При нагревании смеси CaCN2 с NaCl или К. С1 вначале идет обменная реакция б-7 с образованием цианамида щелочного металла, который разлагается 8:
Na2CN2 = NaCN + Na + 72N2
Отравление цианамидами происходит при вдыхании пыли вследствие образования дициана.
Цианамид кальция обладает сильно раздражающими свойствами, вызывает воспалительные заболевания кожи. Он оказывает общее действие на сосудисто-двигательный и дыхательный центры, вызывает головные боли, желудочно-кишечные заболевания и т. п.9- 10. Раздражающее действие цианамида кальция CaCN2 на слизистые оболочки и кожу обусловлено содержанием в продукте окиси кальция.
Цианат калия KNCO хорошо растворим в воде. При продолжительном стоянии водный раствор разлагается с образованием двуокиси углерода и аммиака; в растворе NH4NO3 или NH4C1 в аммиаке превращается в карбамид:
KNCO + NH4N03 = KN03 + co(NH2)2
Роданистоводородная кислота HNCS ниже 0° — бесцветная, быстро желтеющая жидкость с острым запахом, напоминающим запах уксусной кислоты. Сильно летуча, на воздухе легко разлагается на HCN и персульфоциановую кислоту. Разбавленные водные растворы (3—5% HNCS) достаточно устойчивы. В более концентрированных растворах разлагается с образованием CS2 или H2S:
2SCNH + 2Н20 = С02 + CS2 + 2NH, SCNH + 2Н20 = С02 + H2S + NH3
Роданистый аммоний NH4NCS выделяется из водного раствор в виде белых кристаллов, плавящихся при 159°. При 0° в 100 г во ды растворяется 122,1 г, при 20°— 162,2 г роданида аммония. Пр нагревании до 150—220° роданид аммония превращается в тиомо- чевину. В системе NH4NCS—(NH2)2CS переходная точка лежит при 142° и соответствует составу 40% NH4NCS и 60% (NH2)2CS. Предполагают п, что процесс протекает с образованием промежуточного продукта HN=C(SH)NH2. В системе NH4NCS— — (NH2)2CS—Н20 12 помимо основных компонентов кристаллизуется двойная соль NH4NCS - (NH2)2CS.
Роданистый калий KNCS при нагревании на воздухе до 600° разлагается с образованием цианистого калия, синильной кислоты и сернистого газа.
Роданид железа отличается интенсивной кроваво-красной окраской в водном растворе. Это служит характерной реакцией на железо или родан 13.
Цианистые соли обладают большой способностью к комплексо - образоьанию, причем ион CN~ входит во внутреннюю сферу комплекса. Примером комплексных цианистых солей могут служить цинковые цианистые комплексы 14 [Zn(CN)3]~ и [Zn(CN)4]2", образующиеся при растворении цинка в растворах цианидов, а также ферроцианид натрия Na4Fe(CN)6 (железистосинеродистый натрий или желтый синь-натр, или желтая кровяная соль) и феррицианид натрия Na3Fe(CN)6 (железосинеродистый натрий или краен] ш синь-натр, или красная кровяная соль). Эти названия появились в связи с тем, что: 1) ферроцианиды окрашены в желтый, а ферри- цианиды в красный цвет; 2) впервые эти соли получали в промышленности прокаливанием сухой крови животных с щелочными карбонатами и железными опилками; 3) ферроцианиды выделяют из растворов солей трехвалентного железа нерастворимый осадок Fe4[Fe(CN)6]3 ярко-синего цвета (берлинская лазурь), а ферри - цианиды из растворов солей двухвалентного железа выделяют осадок Fe3[Fe(CN)6]г также синего цвета (турнбуллева синь). Берлинской лазури приписывают также формулу Fe[Fe(CN)6]15.
Железистосинеродистый натрий кристаллизуется из водных растворов в виде декагидрата Na4Fe(CN)6-10Н20, а выше 81° — в безводной форме. Насыщенный раствор содержит при 25° 17,04%, при 80° —38,0% Na4Fe(CN)6. Декагидрат на воздухе легко выветривается (давление водяного пара над декагидратом при 25° равно 9 мм рт. ст., а при 60° — 99,5 мм рт. ст.).
Железистосинеродистый калий кристаллизуется с тремя молекулами воды — K4Fe(CN)6-3H20. Растворимость его в воде при 25° составляет 24,15%.
Железосинеродистый калий КзРе(СЫ)6 кристаллизуется безводНым. Растворимость в воде при 4° — 24,8%, при 104,4° — 45,2%.
ПРИМЕНЕНИЕ
Способность цианидов образовывать комплексные соединения широко используется для извлечения драгоценных металлов (золота, серебра) из руд. Ядовитые свойства синильной кислоты используются при применении цианидов в качестве фумигантов для борьбы с паразитами в сельском хозяйстве (окуривание растений) и при санитарной обработке (окуривание пароходов, железнодорожных вагонов, казарм и пр.) 1б_18. Цианиды используют в гальваностегии, в производстве пластических масс, искусственных смол, лаков, красок, для цементации стальных изделий, в текстильной промышленности в качестве протрав при крашении тканей (комплексные соли) и пр. Указывают 19-20, что небольшие добавки комплексных цианидов увеличивают растворимость хлоридов натрия и калия.
Имеются патенты, предлагающие использовать продукты полимеризации синильной кислоты в качестве удобрений 21>22.
Синильная кислота имеет важное значение в качестве исходного сырья для получения акрилонитрила СН2=СН—CN, являющегося полупродуктом в производстве нитрильного каучука и синтетических волокон 23-27. Получаемые из синильной кислоты акрилаты перерабатывают в органическое стекло.
Цианистый натрий и цианистый калий, а также цианплав (черный цианид), получаемый из цианамида кальция (стр. 1525), используют в машиностроении для закалки специальных сталей, для извлечения золота из руд (цианирование руд), при обогащении полиметаллических руд, а также в сельском хозяйстве для борьбы с вредителями и в ряде' других отраслей промышленности и народного хозяйства 28. Особенное значение они имеют для борьбы с сусликами 29 и с вредителями цитрусовых растений 30.
Цианплав служит сырьем для получения цианидов натрия, калия, а также желтой кровяной соли. Последнюю применяют в текстильной промышленности и в производстве красок.
Цианамид кальция используют в качестве азотного удобрения, в особенности под технические культуры — хлопок, сахарную свеклу и др. Предложены различные смеси на основе цианамида кальция с целью увеличения длительности его действия 31>32 или придания ему также инсектицидных и фунгицидных свойств 33. Цианамид кальция в смеси с кремнефторидом натрия применяют для дефолиации хлопчатника перед механизированной уборкой хлопка 34>35. Он обладает также гербицидными свойствами и используется для уничтожения сорняков. Помимо указанных областей применения, цианамид кальция служит исходным материалом в химической промышленности для получения цианплава и цианидов, а также дицианамида, применяемого в производстве пластических масс, искусственных смол и лаков.
Описаны каталитические свойства цианамида кальция, например, при окислении раствора индигокармина перекисью водорода при 35—40° и применение его в качестве активатора и носителя для приготовления активных смешанных контактов36.
Роданид аммония и другие роданиды находят ограниченное применение. Некоторое количество роданида аммония получают при очистке коксового газа. Возможна переработка роданида в тиомочевину 12, употребляемую в различных областях техники. Роданид аммония используется для синтеза роданина37, производные которого находят применение в неорганическом анализе38, фотографии, а также в органическом синтезе для получения аминокислот, нитрилов, аминов39.
Из роданистых солей можно получать полироданоалканы, обладающие инсектофунгицидными и бактерицидными свойствами40.
В табл. 119 приведены качественные показатели, которым должны удовлетворять технические цианистый натрий и цианистый калий.
ТАБЛИЦА 11»
|
Качество технических цианистого натрия (ГОСТ 8464—69) и цианистого калия (ГОСТ 8465—69) (Содержание компонентов в %)
|
Цианид натрия и калия упаковывают в железные барабаны весом до 100 кг или в железные банки весом до 10 кг. Барабаны и банки помещают в фанерные барабаны с дощатыми днищами.
При работе с цианидами натрия и калия необходимо строго соблюдать правила безопасности обращения с высокотоксичными отравляющими веществами. Аппаратура должна быть абсолютно герметизирована. При вскрытии аппаратуры и тары, а также при содержании в воздухе более 0,05—0,06 мг HCN на 1 л необходимо пользоваться противогазом.
Цианплав должен удовлетворять по своему качеству требованиям ГОСТ 452—66 (табл. 120). Цианплав марки А — пластинчатый — применяется для промышленных целей. Цианплав марки Б — молотый — применяется для борьбы с вредителями в сельском хозяйстве, а также как дезинсекционное и противоэпидемическое средство.
ТАБЛИЦА 120
|
. Качество цианплава (черного цианида) по ГОСТ 452—66 (Содержание компонентов в %)
|
Размеры частиц цианплава, применяемого в качестве противоэпидемического средства, должны быть от 0,3 до 3,0 мм. В сельском хозяйстве цианплав применяют в порошкообразном виде с размером частиц от 0,3 до 1,5 мм.
Цианамид кальция выпускают двух марок: грубомолотый (марка А), предназначаемый для переработки в другие химические продукты, и тонкомолотый, умасленный минеральным маслом (марка Б), используемый в качестве дефолианта41. Чистый CaCN2 содержит 34,98% азота. В техническом продукте имеются примеси выделившегося углерода и непрореагировавших СаС2 и СаО (табл. 121).
ТАБЛИЦА 121
|
Требования к качеству цианамида кальция по ГОСТ 1780—56 (Содержание компонентов в 96)
|
Цианамид кальция марки Б, отгружаемый в хлопкосеющие районы Узбекской, Туркменской, Таджикской, Киргизской и Казахской
ССР, упаковывают в барабаны емкостью 50—100 л, при отгрузке в другие районы продукты упаковывают в пятислойные бумажные битумированные мешки весом 35 кг.
Требования к качеству технических железистосинеродистых натрия и калия приведены в табл. 122. Их упаковывают в многослойные бумажные мешки с полиэтиленовым вкладышем или битумированные с непропитанным внутренним слоем бумаги.
ТАБЛИЦА 122
Требования к качеству железистосинеродистых натрия (ГОСТ 6817—54) и калия (ГОСТ 6816—75)
(Содержание компонентов в °/0)
NaiFe(CN)6- ЮН20 или K4Fe(CN)6 X
X ЗН20, не менее..........................................
Хлориды (в пересчете на NaCN),
Не более. ...................................................
Цианиды (в пересчете на NaCN),
Не более ....................................................
Не растворимый в воде остаток. . . Не растворимый в соляной кислоте
Остаток, не более.........................................
Влага, ие более...............................................
|
97 |
95 |
98 |
96 |
|
1,0 |
2,0 |
1.1 |
1 1 |
|
0,01 |
0,02 |
0,001 |
0.001 |
|
0,02 |
. 0,04 |
0,01 |
0.01 |
|
0,01 |
0,03 |
_ |
_ |
|
2,0 |
3,0 |
— |
—- |
|
Железистосинеродистый натрий |
|
1-й сорт. 2-й сорт |
|
Железистосинеродистый калий |
|
1-й сорт |
|
2-й сорт |
СЫРЬЕ
В первый период своего развития (до 90-х годов прошлого века) производство цианидов базировалось почти исключительно на переработке животных и растительных отбросов. В дальнейшем все большее значение стали приобретать синтетические методы, основанные на переработке аммиака, на фиксации атмосферного азота, а также методы, связанные с переработкой отходов коксогазового производства, паточной барды и др. В настоящее время большие количества цианидов производят путем переработки цианамида кальция, и превалирующее значение приобретает синтез синильной кислоты из природного газа (метана) и аммиака.