Полисиликаты щелочных металлов
Если вслед за Айлером [2] полагать, что кремнезем в щелочном растворе с модулем 2 находится в истинно растворенном неколлоидном состоянии, а все содержание кремнезема в растворах сверх модуля более 2 имеет коллоидный характер, то окажется, что в области полисиликатных растворов коллоидный кремнезем составляет от 50 до примерно 92% от общего содержания кремнезема. Размер частиц коллоидного кремнезема и степень их обводненности может быть существенно разной в растворах одного и того же состава и зависит от способа получения.
В монографии [2] указывается, что растворы полисиликата натрия с модулем 4—6 можно получить добавлением раствора жидкого стекла к концентрированному золю кремнезема с размерами частиц 5—25 нм и концентрация кремнезема в растворе может достигать 20% Si02. При этом на начальных стадиях процесса наблюдается гелеобразование, но при старении или непродолжительном нагревании раствор становится прозрачным с невысокой вязкостью. Длительного хранения или нагревания такие растворь1 не выдерживают, в них выделяется кристаллический осадок. Пр^ использовании вместо золя растворов кремневой кислоты с низкоИ молекулярной массой получают растворы полисиликатов натри*
64 с более высокими модулями. Растворы полисиликатов калия проявляют несколько большую стабильность. Использование 30% 51О2 золей и растворов силиката калия с модулем 3 позволяет получить полисиликатные растворы с модулем от 10 и выше, но приливание раствора силиката натрия к такому золю приводит к немедленному загустеванию системы. Вязкий раствор полисиликата калия с модулем около 6 образуется также при осторожном нагревании раствора силиката калия с аморфным кремнеземом.
Нами были получены растворы полисиликатов калия путем приливання по каплям концентрированного раствора КОН к крем - незолю с концентрацией Si02 около 24% при интенсивном перемешивании. Диаметр частиц в исходном золе был около 14 нм. Растворы с модулем меньше 10 к окончанию приливання щелочи становились молочного цвета, но через 6—24 ч восстанавливали прозрачность. Кинематическая вязкость измерялась в день получения раствора.
Результаты исследования полученных растворов представлены в табл. 10. Обнаружено, что многие свойства раствора непрерывно меняются, т. е. растворы представляют собой «живущие» системы. Динамика происходящих изменений в системе прослеживалась путем измерения во времени рН раствора, его вязкости, концентрации растворимого кремнезема (a-Si02, масс. %), определяемой фотоколориметрическим методом [26], снятия ИК-спект - ров раствора и получения на электронном микроскопе снимков дисперсной фазы раствора, адсорбированной на пленке.
|
Таблица 10. Свойства растворов полисиликатов калия
|
|
JO. l ь |
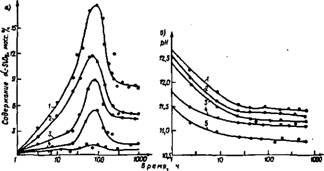
Изменение концентрации растворимого кремнезема (а-БіОг) в системе при ее старении, а также изменение рН раствора приве - Дено на рис. 35 а, б. Во всех случаях содержание а-БіОг на ранних Стадиях процесса взаимодействия золя и щелочи после их смеше - Ния больше, чем на более поздних стадиях. Характер изменения концентрации растворимого кремнезема носит, таким образом, Экстремальный характер. Поверхность дисперсной фазы со време - нем возрастает, а не уменьшается. Узкая полоса поглощения в ИК-спектре с минимумом 1140—1150 см-1, характерная для термически обработанного безводного золя, практически исчезает
® Заказ 23 се
|
Рис. 35. Изменение a=Si02 (а) и рН (б) при старении калиевых полнсиликатиых растворов Модуль раствора: / — 3,9; 2 — 5,2; 3 — 6,5; 4 — 9,3; 5 — 38,8 |
|
|
|
2 4 6 8 Я) 12 Ft Ю в Время существования растворов, сут |
|
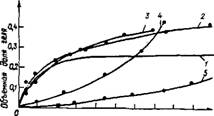
Рис. 36. Кинетика гелеобразования в растворах полисиликатов калия с разными модулями (см. рис. 35) |
Для низкомодульных полисиликатных растворов и примерно ь времени достижения максимума, смещаясь в низкочастотную об ласть и расширяясь, охватывает диапазон 980—1110 см"1. На бо лее поздних стадиях старения эта широкая полоса поглощен® сужается, и ее минимум охватывает область 1040—1100 см" Не углубляясь в детали результатов проведенного исследова ния, остановимся только на сущности происходящих при жиз№ Полисиликатных растворов процессов. При добавлении щелочі к золю она быстро усваивается, так что рН раствора не соотвеї ствует концентрации прибавленной щелочи, но растворимые фор мы кремнезема начинают возрастать гораздо, позже. Вероятна прибавленная щелочь переводит золь в раствор в форме, близко* к мономерной. При достаточно высокой концентрации низкопол' мерных форм кремнезема усиливаются их конденсация и гидролИ-' это высвобождает гидроксильные ионы, которые снова вступав в реакцию растворения исходного золя. Этот процесс в итоге пр11 водит к образованию фазы полимерного кремнезема, которая о1 личается от исходной более высокой степенью гидратации. Пс верхность вновь образующейся фазы гидратированного кремнез( ма велика, и поэтому удельная поверхность кремнезема расте1 flo нашим расчетам, 1 моль ОН- ионов переводит в раствор примерно в 2 раза больше молей SiC>2. Частицы новой фазы не увеличиваются до больших размеров, а, как это свойственно самопроизвольно образующимся кремнезолям, останавливаются в росте, достигнув порядка 5—7 нм. Фазу, сформированную из таких частиц, можно видеть на снимках с электронного микроскопа.
Термодинамической основой такого процесса перехода от безводных форм к гидратированным является повышенная растворимость безводных золевых частиц по отношению к гидратным формам полимерных силикатов. Поверхность вновь образующейся фазы, по нашим оценкам, составляет 1500—2000 м2/г. Скорость процесса затухает в течение 1—5 сут в связи с уменьшением рН раствора и появлением отрицательных зарядов на вновь образующейся поверхности или, иными словами, за счет адсорбции гидроксильных ионов на растущей фазе. Описываемый процесс соответствует многочисленным наблюдениям при определении растворимости кремнезема в щелочных средах, когда во многих случаях равновесная концентрация кремнезема устанавливается сверху, т. е. со стороны пересыщенных растворов. Такого же рода процесс происходит при гидратации цементных фаз, где раствор оказывается пересыщенным по отношению ко вновь образующимся гидратным формам силикатов. В высокомодульных полисиликатных системах к моменту затухания процесса большая часть кремнезема остается в исходном безводном состоянии. Таким образом, полисиликатный раствор, образованный добавлением к золю концентрированной щелочи, состоит из уменьшившихся в размерах частиц исходного золя, высокодисперсной фазы гидратированного кремнезема с размерами частиц не выше 5—7 нм и кремнезема, находящегося в растворе в виде ионных олигомерных форм.
Плотные, не растрескивающиеся при высыхании пленки и блоки из высокомодульных силикатных систем можно получить, по Айле - ру, подбором частиц кремнезема разных размеров, скрепляемых этим растворенным кремнеземом, располагающимся в пустотах. Описанный процесс растворения золей в растворах щелочей следует принимать во внимание при составлении таких композиций.
Растворение активных форм кремнезема в щелочах при повышенных температурах должно протекать, видимо, иным образом, и свойства образующихся систем будут иными. Упоминавшиеся выше вязкие растворы полисиликатов калия, образованные при температурах около 100 °С растворением аморфного кремнезема, Отличаются от рассмотренных нами именно величиной вязкости. Растворы полисиликатов натрия или калия, полученные добавлением к низкомодульному раствору в рассчитанном количестве Катионитов в кислотной форме, будут лишены негидратированной Части кремнезема, а самопроизвольно образовавшаяся высоко- Дисперсная фаза гидратированного кремнезема будет иметь значительно более высокую концентрацию, что должно повлиять на Вязкость системы и ее устойчивость к гелеобразованию. Срок
Жизни таких полисиликатных растворов, особенно высокомодуль-
Иых должен уменьшаться.
Жизнь полученных нами растворов полисиликатов калия не заканчивается растворением части кремнезема и переходом его в гидратированные формы, что происходит в течение нескольких суток. Позднее начинают развиваться процессы гелеобразовання, и система теряет текучесть, что фиксировалось нами измерением вязкости системы, изменение которой отражало процессы гелеобразовання. Растворы, будучи маловязкими, длительное время сохраняли ньютоновский характер течения. В связи с этим изменение вязкости в процессе гелеобразовання трактовалось с позиции классических представлений, разработанных Эйнштейном. Образование цепочек взаимодействующих частиц кремнезема, ветвясь и разрастаясь, создает вместе с гидратными оболочками относительно неподвижные области, которые, увеличиваясь в объеме, приводят к застудневанию, которое наступает, когда фаза геля приближается к половине общего объема системы. Рассчитав по величине вязкости долю объема фазы геля, мы получили кинетику гелеобразовання, представленную на рис. 36.
Обращает на себя внимание различный характер кривых для низкомодульных и высокомодульных растворов. Высокомодульные системы сохраняют кинетику, характерную для золей. Для них скорость образования геля примерно пропорциональна поверхности фазы геля, следовательно с ростом поверхности скорость непрерывно нарастает. Константа скорости гелеобразовання зависит от ионной силы раствора и увеличивается с уменьшением модуля раствора. Низкомодульные системы имеют затухающую кинетику, а высокощелочные системы оказываются стабильными. Между стабильными золями и стабильными низкомодульными растворами находится область наименее устойчивых растворов. Следует иметь в виду, что исследованные нами системы не были свободны от ионов натрия. Полисиликаты натрия менее устойчивы по отношению к кристаллизации или гелеобразованию, чем калиевые, особенно в области высоких рН. Для проявления большей устойчивости калиевых систем они должны быть достаточно чистыми от натрия.
Нами исследована зависимость свойств полисиликатных растворов от концентрации при одном и том же модуле (табл. 11)- Растворы были получены разведением дистиллированной водой калиевого жидкого стекла модуля 3,31 и концентрации 21,6% Si02 с последующим добавлением натриевого кремнезоля до общего модуля 5 при комнатной температуре. Старение растворов длилось 1 сут. Кинематическую вязкость измеряли иа шестой день после получения раствора.
При хранении в наименее концентрированном растворе выпадает небольшой осадок, и процесс загустевания визуально ближе к коагуляции. Вероятно, образование осадка приводит к снижений содержания a-Si02- Как следует из табл. 11, использование разбавленного жидкого стекла при образовании полисиликатног0
|
Таблица 11. Свойства волисиликатиых растворов Разной концентрации
|
|
12,7 |
3,82 |
0,10 |
1,155 |
7,60 |
11,36 |
1,9 |
93 |
|
15,6 |
4,70 |
0,13 |
1,191 |
9,25 |
11,36 |
3,0 |
84 |
|
17,6 |
5,31 |
0,15 |
1,226 |
9,33 |
11,36 |
4,4 |
43 |
|
19,1 |
5,76 |
0,16 |
1,242 |
9,08 |
11,36 |
4,7 |
27 |
|
20,3 |
6,10 |
0,17 |
1,259 |
9,00 |
11,36 |
8,2 |
17 |
|
21,6 |
10,2 |
— |
1,300 |
19,5 |
11,78 |
14,2 |
— |
|
18,3 |
— |
0,78 |
1,124 |
0,78 |
10,77 |
1,8 |
|
Примечание. В последних двух строках приведены физико-химические характеристики использованного калиевого жидкого стекла и натриевого кремиезоля. |
|
Таблица 12. Свойства растворов полисиликатов лития
4,8 20 2,1 1,17 1,2 < 11,0 12 8,5 20 1,2 1,17 0,8 11,0 12 |
Раствора практически ие меняет таких характеристик, как содержание a-SiC>2 и рН раствора, что косвенно свидетельствует о неизменности полимерного состава. Вязкость полисиликатного раствора меняется симбатио с изменением вязкости жидкого стекла при разбавлении.
Литиевые полисиликатные растворы существенно отличаются по свойствам (табл. 12). Они могут быть получены во всем диапазоне модулей добавлением LiOH к раствору поликремневой кислоты, или к кремнезолю, или к суспензии геля кремнезема, если системы свободны от других катионов. Образующаяся густая масса за несколько часов при комнатной температуре самопроизвольно разжижается, образуя устойчивые растворы. При длительном нагревании этой массы разжижения не наступает.
Помимо высокой устойчивости, литиевые растворы гораздо более совместимы с водорастворимыми органическими веществами, чем натриевые или калиевые. Айлером исследованы состарившиеся 8 течение недели системы водных полисиликатов лития, получение смешением растворов низкомолекулярной кислоты и гидроокиси лития. В этих системах определяли изменение содержания Растворимого кремнезема во времени. По скорости взаимодействия Юлисиликатов лития с молибденовой кислотой было определено, Что размер коллоидных частиц, самопроизвольно образовавшихся пРи получении полисиликатов, увеличивается с возрастанием мо - ДУля. Эта связь прослеживается до модуля 10. Отсюда следует, что в низкомодульных полисиликатных системах размер частиц опре - деляет равновесие в системе с данной щелочностью. Негидра, тированной частице кремнезема диаметром 0,9 нм соответствует число атомов кремния 8, для диаметра 1,5 нм — 40, для 3 нм 300. Степень полимеризации кремнезема с возрастанием диаметра частицы растет чрезвычайно быстро, и здесь, на переходе к коллоидным системам, утрачивается однозначная определенность между составом раствора и размером частиц кремнезема.
В отличие от Айлера, нами был получен ряд полисиликатных растворов лития растворением в щелочи высокополимерных форм кремнезема: различных золей и аэросила с удельной поверхностью 175 м2/г, а также растворением щелочи в золях. Золи имели средний диаметр частиц 10—13 нм и были стабилизированы натриевой или литиевой щелочью. После смешения компонентов образовывалась густая масса, которая разжижалась на 2—4-е сутки старения при комнатной температуре. На 3—5-е сутки раствор полиСиликата из золей просветлялся до небольшой опа - лесценции, а из аэросила — оставался непрозрачным молочного цвета, т. е. состоял из слишком крупных частиц. Все растворы содержали 20 масс. % БіОг-
Растворы полисиликатов, полученные из золей, анализировали на содержание Si02 по двум методикам. Титрованием соляной кислотой с NaF (см. 4.2.1) находили содержание золевой составляющей Si02 в растворе. Предварительным титрованием этим методом исходных золей было определено, что хорошо сформированные частицы золя не титруются и содержание растворенного Si02 в исходных золях не превышает 0,2 масс. %. По известной методике определения Si02 с образованием желтого кремнемо - либдатного комплекса снимали кинетическую кривую образования этого комплекса в состарившихся растворах полисиликатов за первые 30 мин реакции. С молибдатом кремнезем взаимодействует только в мономерной форме, поэтому полученная кинетическая кривая представляет суммарный результат взаимодействия мо - либдата с мономерным кремнеземом, бывшим в растворе и деполи- меризовавшимся за время реакции. Константы скорости деполимеризации различных полимерных форм по реакции первого порядка собраны Айлером [2]. Из их анализа следует, что различные формы кремнезема со степенью связности 2, силоксановые связи которых практически равнодоступны для атаки реагентами, вступают в реакцию с молибдатом за первые 5—10 мин реакции. Действительно, по истечении этого времени скорость образования желтого комплекса стабилизируется, и ее легко зафиксировать по кинетической кривой. Это дает возможность сосчитать константу скорости реакции первого порядка взаимодействия оставшегося высокополимерного кремнезема с молибдатом, рассчитать начальную концентрацию этих полимеров и по константе скорости оце- нить степень их полимерности. Таким образом, весь кремнезем в растворе полисиликата можно количественно расчленить на тр11
составляющие: a-SiCb — мономерный кремнезем, цепочечные и цикличные олигомеры; 7-Si02 — остатки золя, не титрующиеся с NaF; P-Si02 — вновь образовавшиеся в результате взаимодействия золя со щелочью высшие полимеры. Их относительное содержание приведено в табл. 13.
Рис. 35), содержание ct-SiCb в первый период оказывается значительно выше, чем в последующем, и в течение 100 сут наблюдаются затухающие колебания a-формы кремнезема. Видимо, растворение золя в щелочи идет через образование мономеров в растворе, которые со временем полимеризуются, но, в отличие от золя, при комнатной температуре сохраняют гидратированную форму и легко титруются с NaF. Все синтезированные растворы полисиликатов лития сохраняются больше года. Таким образом, растворы полисиликатов лития, приготовленные из высокополимерных форм кремнезема, при комнатной температуре отличаются от растворов, приготовленных из малополимерной кремневой кислоты, наличием золевой составляющей, которая длительно сохраняется в растворе.
В реальной технологической практике для натриевых и калиевых систем существует также множество экспериментальных Данных, показывающих, что даже при модулях еще более низких, чем модули полисиликатных растворов, размер и состояние коллоидных частиц могут быть различны.
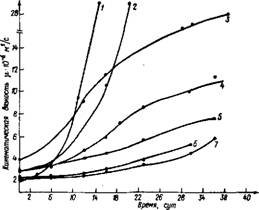
Литиевые полисиликатные растворы используются главным °бразом в качестве связующего в цинковых антикоррозионных покрытиях, обеспечивая устойчивость красок и длительность их хРанения. Кроме того, эти растворы пригодны для нанесения тонких кремнеземных пленок на различные поверхности, в том чис^ на поверхности стекол оптических приборов. Гидроокись ЛИТИЯ і также силикат или полисиликат лития полезны как добавка. натриевым или калиевым силикатным системам, модифицируя Лх свойства. Одним из таких свойств является устойчивость поли - силикатной системы, которую часто требуется менять в ту или иную сторону в различных технологиях. С этой целью был опробован ряд добавок к растворам полисиликата калия и исследовано изменение кинематической вязкости растворов во времени (рис. 37) Введение катионов тетраэтиламмония (ТЭА) резко увеличивает устойчивость полисиликатной системы по отношению к гелеобразо - ванию. В малых дозах бромиды и гидроксиды ТЭА малоразличимы по эффекту действия. В больших дозах они перестают быть эквивалентными, так как бромиды значительно увеличивают ионную силу раствора и тем понижают стабилизирующее действие катионов. Гидроксиды четвертичного аммония в отличие от бромидов усваиваются полисиликатной системой, несколько понижая ее общий модуль, но не влияя на стабилизирующий эффект. Среди органических катионов тетраэтиламмоний не является наилучшим по своему действию. Айлер приводит ряд других, более сложных катионов, которые можно вводить в значительно меньших пропорциях, доводя отношение Si02/ (R4N) 20 почти до 103, для достижения того же результата. На основе некоторых силикатов четвертичного аммония приготавливают устойчивые полисиликатные растворы, которые могут быть высушены с образованием аморфных порошков, имеющих модуль до 20. Такие порошки способны
|
Рис. 37. Изменение кинематической вязкости растворов полисиликатов калий (% Si02) с модулями 5 и 10 во времени при добавлении тетраэтиламмония в виДе Бромида (Б) или 30% раствора гидроксида (Г) / — л= 10 без добавки; 2 — п=5 без добавки; 3 — п—5+5% Б; 4 — п=5+ I % Б; 5" 1=5+1% или 5% Г; 6 — п= 10+1% Б; 7 —/1=10+1% Г |
Быстро растворяться в воде, образуя вновь полисиликатный раствор. Это означает, что в таких системах процессы агрегации частиц кремнезема не происходят при любых концентрациях последнего, g некоторых модификациях содержание Si02 в водорастворимых порошках превышает 70 масс. %.
Необходимо отметить, что близкие по химической природе третичные амины, в том числе такие, как триэтаноламин, обладают очень слабым стабилизирующим действием. Видимо, для стабилизации отрицательно заряженных мицелл кремнезема в полисиликатных растворах важна именно ионная форма. Более подробно полисиликатные системы на органических основаниях рассматриваются в разделе 2.6. Гликоли, такие как этиленгликоль, пропилен - гликоль, а также глицерин, добавленные в малых количествах (менее 1%), мало влияют на скорость гелеобразования, а в больших дозах (около 5%) существенно ускоряют образование геля.