Теплофизические, электрические и другие свойства
Сведения о таких физических свойствах пластификаторов как дипольный момент, термический коэффициент линейного расширения, диэлектрическая проницаемость очень ограничены (см. табл. 3.15). Информация о различных формах теплового расшире-
Та блица 3.15. Физические свойства пластификаторов [22, 23, 24, 38]
|
Пластификатор |
Дипольный момент при 20 °С |
Поверхностное натяжение а-Ю3, Н/м |
* Термический коэффициент линейного расширения При 20 °С, а-10-j |
Диэлектрическая Проницаемость прн 20 °С |
|
Диметил-о-фталат |
2,62 |
_ |
____ |
|
|
Диэтил-о-фталат |
2,83 |
37 (при 20 °С) |
— |
— |
|
Ди-и-бутил-о-фталат |
2,82 |
35,6 (при 25 °С) |
78 |
— |
|
Ди (2-этилгексил) - о-фталат |
— |
33 (прн 20 °С) |
74 |
4~6 |
|
Диизодецил-о-фталат |
— |
29 (при 20 °С) |
80 |
|
|
Дитридецил-о-фталат |
— |
— |
— |
5,2 |
|
«-Бутилбекзил-о-фталат |
— |
39,9 (при 25 °С) |
— |
— |
|
Ди (циклогексил) - о-фталат |
— |
36,4 (при 75 °С) |
— |
— |
|
Ди (2-этилгекСил) адипинат |
— |
29 (при 20 °С) |
— |
4,4 |
|
Трикрезилортофосфат |
— |
— |
120 (при |
— |
|
- |
* |
50—100 °С) |
|
Таблица 3.16. Поверхностное натяжение триарилортофосфатов при различных температурах [9, 10]
|
Ния низших диалкил-о-фталатов. при 20°С, выраженная в виде дипольных моментов, получена путем определения радиочастотных диэлектрических спектров релаксации поглощения.
Экспериментальные данные о динамических диэлектрических свойствах позволяют предположить, что диалкил-о-фталаты при комнатной и близких к ней температурах существуют в виде смеси двух конформеров, различающихся поворотами плоскостей ал- коксикарбонильных радикалов относительно плоскости СбЬЦ-коль - ца [38].
В работах [9, 10] приведены данные об изменении поверхностного натяжения и парахора в зависимости от температуры для триарилортофосфатов. Поверхностное натяжение определяли методом капиллярного поднятия (табл. 3.16). Для интервала температур 20—240 °С поверхностное натяжение можно определить по уравнениям:
Для трикрезилортофосфата
А = 40,09 — 0,09331 (коэффициент корреляции 0,9954)
Для три-п-крезилортофосфата
А = 40,2J — 0,0748/ (коэффициент корреляции 0,9871)
Значение парахора рассчитывали по уравнению Сегдена: ;
Трикрезилортофосфат
Температура, °С........................................ '20 100 170
Парахор..................................................... 773 781 787
Три-п-крезилортофосфат
Температура, °С... . . 85 130 180 Парахор 788 795 797
3.2. ФИЗИКО-ХИМИЧЕСКИЕ СВОЙСТВА 3.2.1. Гидролиз, алкоголиз, ацидолиз
Сложноэфирные пластификаторы представляют собой нейтральные соединения и за исключением эфиров со свободными гидроксильными группами очень мало растворяются в воде. Однако под влиянием влаги они медленно (а при действии оснований или кислот значительно быстрее) распадаются на исходные компоненты: кислоты и спирты.
При длительном пребывании сложных эфиров в воде происходит их омыление с образованием кислоты. Поскольку гидролиз сложных эфиров катализируется кислотами, то дальнейший процесс протекает автокаталитически [39].
Протекание гидролиза сложных эфиров в кислой среде во времени носит довольно сложный характер, так как реакция катализируется не только ионами Н+, но и другими кислыми частицами, присутствующими в реакционной массе, а также водой. С помощью изотопного метода и путем изучения стерической конфигурации реагирующих соединений установлено, что гидролиз
сложного эфира карбоновой кислоты может протекать с разрывом ацил-кислородной связи по бимолекулярному механизму АсАг с передачей протона Н+ от иона кислоты катализатора спиртовому атому кислорода и нуклеофильной атакой молекулы воды на карбонильный атом углерода [40, 41].
При щелочном гидролизе нуклеофильная атака гидроксильным ионом происходит по карбонильному атому углерода молекулы сложного эфира (механизм АСВ2). Все стадии реакцир обратимы, кроме стадии, на которой образуется карбоксилатный ион, не присоединяющий протон. Однако реакция переэтерификации эфира спиртом в отсутствие воды обратима и катализируется ионом ал - коголята.
Щелочной гидролиз по механизму AjBt протекает тем легче, чем устойчивее образующийся анион и карбкатион. При медленной ионизации эфира:
О О
II II
R—С—OR ■<—* R-C-O- + R+
Карбокатион взаимодействует далее с растворителем — водой:
R+ + Н20 -------- ROHP + H+
(R'COO" + Н+ ■<—RCOOH)
По этому механизму протекает, например, гидролиз оптически- активного кислого эфира фталевой кислоты: СН3СН=СН О О
I II II
СН—О—С—Свн4—с—ОН
I
СН3
|
|
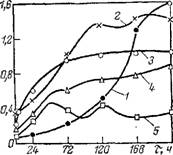
Результаты исследования гидролиза сложноэфирных пластификаторов в водной среде представлены на рис. 3.7. В зависимости от строения кислотной части эфира ароматических дикарбоно - вых кислот алкилтетрагидрофталаты являются более гидролитически стойкими, чем о-фталаты [42]. Изменение кислотного числа эфиров трех тетрагидрофталевых кислот, установленное при нагревании навески образца эфира (2,5 г) с водой (2,5 г) в ампуле при 100 °С в течение 216 ч, показывает, что их гидролиз резко отличается от гидролиза ди-2-этилгексил - о-фталата (рис. 3.7). Гидролиз ди-2- этилгексил-о-фталата носит автока - д-
Рис. 3.7. Изменение кислотного числа эфиров в процессе гидролиза при 100°С:
/ — ди (2-этилгексил) фталат; 2 — ди (2-этилгексил) - тетрагидрофталат; 3 — ди(2-этилгексил)-3-метил - тетрагидрофталат; 4 — ди(2-этилгексил)-4-метил - тетрагидрофталат; 5 — ди-н-иоиил-3-метилтетрагнд - рофталат.
|
Таблица 3.17. Константы скорости (&.10~2, мин~') реакций кислотного и щелочного гидролиза полиэфирных пластификаторов общей формулы [43] C4H9OOC(CH2)4CO[OROOC(CH2)4CO]OC4H9 (где R-остаток гликоля)
|
Талитический характер [39]. Вследствие того, что гидролиз в отсутствие кислого катализатора протекает под влиянием кислоты, присутствующей в эфире, скорость гидролиза повышается с увеличением содержания свободных карбоксильных групп. Кинетическая кривая гидролиза эфиров тетрагидрофталевых кислот носит скачкообразный характер. Повышение стойкости к гидролизу эфиров тетрагидрофталевых кислот авторы работы [42] относят за счет присоединения образующихся при гидролизе карбоксильных групп по двойной связи циклогексенового кольца. Взаимодействие карбоксильных групп с двойной связью протекает легче за счет электронного эффекта метильной группы в молекуле метилтетра - гидрофталевой кислоты по сравнению с фталевой.
Стойкость к гидролизу полиэфирных пластификаторов зависит от их состава и условий проведения гидролиза [43]. В табл. 3.17 приведены значения констант скоростей реакции кислотного и щелочного гидролиза полиэфирных пластификаторов. Из этих данных следует, что с увеличением содержания метиленовых групп в гликольной составляющей (ряд алкиленгликолей) наблюдается снижение скорости гидролиза. Присутствие простой эфирной связи в гликольной составляющей (полиэфирные пластификаторы на основе диэтиленгликоля и триэтиленгликоля) значительно уменьшает стойкость полиэфирных пластификаторов к гидролизу.
Полиэфирные пластификаторы на основе изогликолей (пропи - ленгликоль-1,2; бутандиол-1,3) отличаются значительной стойкостью к гидролитической деструкции.-
Стойкость полиэфирных пластификаторов к гидролизу значительно возрастает при переходе от алифатических к ароматическим составляющим. Так, дибутиловый эфир полидиэтиленгли- кольфталата имеет константу скорости щелочного гидролиза почти на порядок меньшую, чем дибутиловый эфир нолидиэтиленгли - кольадипината.
При полном гидролизе полиэфирных пластификаторов образуется дикарбоновая кислота, гликоль и спирт (или монокарбоно - вая кислота в зависимости от типа полиэфира). Наличие связи
дикарбоновая кислота — гликоль и дикарбоновая кислота — спирт или монокарбоновая кислота — гликоль несколько изменяет механизм гидролиза полиэфирных пластификаторов по сравнению с полиэфирами, получаемыми только на основе дикарбоновых кислот и гликолей.
В работе [44] методом ЯМР исследован гидролиз полиэфирных пластификаторов с концевыми бутоксильными и метоксиль - ными группами с учетом числа связей кислота — гликоль и кислота-— спирт в цепи полиэфира. Результаты расчета позволили оценить влияние природы концевых групп и гликольной компоненты на ход гидролиза полиэфирных пластификаторов.
В полиэфирах с концевыми н-бутоксильными группами более стойкой к гидролизу является связь кислота — спирт (адипиновая кислота — бутанол), причем заметное возрастание числа разорванных связей кислота — спирт у обоих полиэфиров происходит тогда, когда доля разорванных связей кислота — гликоль (адипиновая кислота — гликоль и адипиновая кислота — 2,2-диметил - пропандиол-1,3) достигает примерно одного и того же значения (~0,15), т. е. определенного «порогового» значения кислотности системы, выше которого начинается гидролитический распад связей адипиновая кислота — бутанол.
Гидролизу сложных эфиров ортофосфорной кислоты посвящены многие фундаментальные работы [45—50, с. 47—61]. На гидролиз ортофбсфатов влияют многие факторы (природа заместителя в молекуле эфира, температура, рН-среды, наличие растворителей и пр.). Поэтому механизм протекания этого процесса носит сложный характер. В зависимости от природы аниона и катиона, участвующих в гидролизе, различают: гидролиз (Н+ и ОН"), кислотный гидролиз (Н+ и А~), щелочной гидролиз (К+ и ОН-) я галолиз (образование соли К+ или А-).
Исследование гидролиза ряда эфиров ортофосфорной кислоты в основном указывает, что щелочной гидролиз протекает с разрывом Р—О-связи, а кислотный С—О-связи [45], т. е. высокая нук - леофильность гидроксильного иона в щелочных средах способствует его атаке на атом фосфора с разрывом Р—О-связи. В кислой среде молекула воды обладает меньшей нуклеофильностью и способна лишь к атаке на алкоксильный радикал, что заканчивается разрывом С—О-связи. Возможное протонирование эфирного кислорода, предшествующее алкилированию, способствует в этом случае нуклеофильной атаке.
Так, в работе [46] было показано, что в нейтральной или кислой среде триметилфосфат гидролизуется с расщеплением С—О - связи, а катализа кислотой не наблюдается. В щелочной среде протекает реакция с ионами гидроксида с расщеплением связи Р—О.
|
97: |
Аналогично трифенилфосфат гидролизуется в щелочной среде с расщеплением Р—О-связи. Эта реакция имеет низкую энергию активации (42 Дж/моль) и обмена изотопов при фосфорильном атоме кислорода не происходит.
7—2207
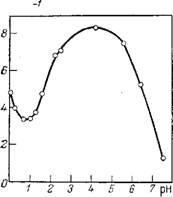
Рис. 3.8. Зависимость скорости гидролиза монометилфосфата при 100 С от рН среды.
Для различных ортофосфатов с уменьшением рН-среды скорость гидролиза проходит через максимум, причем кинетика гидролиза подчиняется закономерностям общего кислотного Катализа [46—48] (рис. 3.8).
Скорость гидролиза в зависимости от природы заместителя изменяется незначительно.
Авторы работы [8], исследуя гидролитическую стойкость полных ортофосфатов при температуре кипения воды в течение 24 ч, установили, что алкилдикрезилортофосфаты более стабильны, чем ал - килдифенилортофосфаты. В ряду изомерных алкилдиарилортофос - фатов эфир с нормальным алкильным радикалом менее стоек к гидролизу, чем с разветвленным радикалом. Максимальной стойкостью к гидролизу обладает эфир, в котором оба атома водорода у p-углеродного атома алкильного радикала замещены метальными группами. По мнению авторов [8], это является следствием большего блокирующего эффекта метальных групп по сравнению с атомами водорода. В общем, смешанные алкиларилортофосфаты занимают промежуточное положение между триалкил - и триарил - ортофосфатами, хотя отдельные эфиры имеют гидролитическую стойкость, эквивалентную этим соединениям.
|
V-10, с |
Ниже приведены данные о стойкости к гидролизу полных эфиров ортофосфорной кислоты [8]:
|
Количество 1 н. NaOH, мл/моль |
|
Количество 1 и. NaOH, мл/моль |
Алкилдифенилортофос- фат «-бутил 2-метилпропил - 2-метилбутил - 2,2-диметилпропил - к-гексил- 2-метилпентил - 2-этилбутил-
«-ОКТИЛ- .
|
27,8 7,3 15.4 1,6 16.5 2.7 4.8 14.6 7,6 3,6 |
6-метилгептил - 2-этилгексил-
Алкилдикрезилортофос фат
И-гексил- • 2-этилбутил - . и-октил - 2-этилгексил - и-децил - . 2-этилоктил-'.
|
4,5 2.3 4.4 1,7 3,3 2,9 4,0 0,2 1,2 |
Симметричные ортофос фаты и-бутил - . 2-этилгексил - крезил-