АКТИВАЦИЯ И ИНАКТИВАЦИЯ НАТРИЕВОЙ ПРОВОДИМОСТИ
Обратимся теперь к модельной теории активации и инактивации Na-проводимости. Такая теория предложена в работах [67—70].
В опытах на аксоне кальмара, проведенных методом фиксации напряжения на мембране, Ходжкин и Хаксли установили экспоненциальную зависимость между величиной начального изменения мембранного потенциала ф и пиковым значением натриевой проводимости gNa [5І]. Изменению ф на 4—6 мВ в сторону деполяризации отвечает е-кратное повышение gNa - Можно предположить, что изменения ионной проводимости являются результатом влияния электрического поля на положение каких-то ионов в мембране. Считая, что проводимостьgNa пропорциональна доле этих ионов, смещенных мембранным потенциалом из исходного положения, получаем
А = gna' m. ax (4 51)
Na 1 + 6 ехр (- zciq&IRT) v4
Где 2 — валентность гипотетического иона, а — число, выража' ющее долю напряжения ф, действующего на ион при его перемещении, b — множитель, не зависящий от ф. В области ф<0 получаем асимптотически
In gNa fa const - f zay@~jRT. (4.52)
Из Начального угла наклона экспериментальной прямой lngNa^) получается za ж 6 [51]. Параметр га можно определить также из центральной части кривой (4.51) по ее наклону в точке gNa = 0,5gNa, max [67]. Формула (4.51) хорошо согла - суется с многочисленными экспериментальными данными, полученными на различных аксонах [71—73]. Параметр za, найденный по (4.52), имеет, согласно этим работам, значения от 3,6 до 6, по (4.51) —от 2 до 4,4. Среднее значение za равно 3,5.
Как уже сказано (см. стр. 178), Ходжкин и Хаксли предполагали, что эти гипотетические ионы определяют активацию и инактивацию каналов для натрия и калия. Была высказана ги* потеза о том, что эти ионы — ионы Са**. Действительно, известно, что изменения концентрации Са++ сильно влияют на возбудимость нервных и мышечных клеток [74] (см. гл. 5). Было показано, что при пятикратном изменении концентрации ионов Са++ кривые зависимости gNa, gK и инактивации от <р смещаются вдоль оси напряжения на 10—15 мВ. Понижение Сса смещает кривые в сторону меньших ф. Концентрация Са++ в растворе сильно влияет на скорость уменьшения gNa при снятии деполяризации. В цитируемой выше работе было выдвинуто предположение о блокировании каналов в мембране ио-
7 М. В. Волькенштейн нами Са++. Отношение доли р каналов, закрытых кальцием, к доле открытых каналов 1 —р
РІІ1 - р) ОО сса ехр (- 2щТ! НТ), (4.53)
Где ссф— напряжение, под влиянием которого ионы Са++ перемещаются от внешнего раствора к месту закрытия канала. Если это место расположено в середине мембраны, то а = 0,5, если у внутреннего края, то а = 1,0. Согласно (4.53) е-кратное изменение Сса эквивалентно изменению ф не менее, чем на 12,5 мВ (если ее = 1,0). Между тем опыт дает от 4,5 до 9 мВ [71—73,75].
Вторая трудность «кальциевой гипотезы» связана со значением га в формуле (4.51). а всегда меньше 1, 2 для Са++ равно 2. Между тем из экспериментального значения га « 3,5 следует, что 2 > 4. Предположение о том, что в блокировке каналов участвуют пары ионов Са++ наталкивается на существенное противоречие — получается смещение кривой ^fNa (ф) , значительно превышающее наблюдаемое на опыте [67].
В работах [6, 19] исследовалось возбуждение мембраны аксона с помощью метода перфузии. Было установлено, что разбавление внешнего раствора изотоническим неэлектролитом повышает потенциал покоя. Аналогичное разбавление внутреннего раствора не оказывает влияния. Напротив, замена С1_ во внешнем растворе на Вг~, SOI'h т. д. не влияет на потенциал покоя, а во внутреннем растворе она влияет на него. Следовательно, на внешней стороне мембраны имеется много фиксированных отрицательных зарядов, а на внутренней их мало. Возрастание внешней концентрации двухвалентных катионов стабилизует состояние покоя, а ее уменьшение приводит к заметным флуктуациям мембранного потенциала. Ионы Са++ оказываются необходимыми для сохранения мембраны в состоянии покоя. На этих основаниях предполагается, что мембрана обладает свойствами катионообменника — в состоянии покоя доступные для обмена отрицательно заряженные центры на внешней стороне мембраны заняты двухвалентными ионами Са++. При стимуляции возникает ионный обмен. Процесс возбуждения можно считать подобным фазовому переходу макромолекул мембраны из одной устойчивой конформации в другую. Обмен ионов Са++ на Na+ развивается кооперативно. Возбуждение триггерно стимулируется переносом внутрь ионов Na+, замещающих внешние ионы Са++, причем изменяется физико - химическая структура мембраны.
Проведем, пользуясь методом молекулярного поля, анализ статистической модели возбудимой мембраны [67]. Представим мембрану как совокупность периодически расположенных ячеек, каждая из которых может находиться в проводящем или
непроводящем состоянии. Проводимость мембраны пропорциональна доле ячеек, находящихся в проводящем состоянии. Предположим, что энергия взаимодействия двух соседних ячеек равна ец, если их состояния одинаковы, и ею, если они различны. Разность е = ец — ею является параметром кооператнвностн. Каждая ячейка может присоединить ион валентности г, который при перемещении из раствора в мембрану пересекает поле с разностью потенциалов аф. Присоединение иона изменяет энергию ячейки на U + za<$9~ (в расчете на моль) и делает ячейку непроводящей. В приближении молекулярного поля получаем
Ехр [ve (2р - 1 )/RT] ОО сса ехр (- zayP/RT), (4.54)
1 - р
Где v — координационное число. Это выражение совпадает с (4.53) в отсутствие кооперативности (при е = 0). Из (4.54) следует, что
(4.55)
(4.56)
Dp
P=0,5 2 (2 — p) ' ^ RT '
D(ygriRT) а так как gNa оо 1 — р, то
D (gNa/gNa, max)
D (фST/RT)
SNa^O'SSNa. max 2 ^ ^
В отсутствие кооперативности, т. е. при р = 0, эта производная равняется га/4. Как уже сказано, опыт дает za « 3,5. Такой же наклон кривой gNa(f) можно получить из формулы (4.56) при любых га < 4, если задать соответствующее значение р > 0. Таким образом, наклон кривой ^а(ф) можно объяснить при г = 2. Однако смещение кривой при изменении Сса с этим не согласуется. Из (4.54) следует условие смещения кривой
1п сса — zaq>!F/RT = const
И величина изменения ф при е-кратном изменении Сса равна Аф — 25/га (в мВ) независимо от значения р. Совпадение этого значения Дф с опытом получается лишь при za т 3,5.
Отсюда следует, что одновременное объяснение двух, несомненно связанных друг с другом эффектов, — формы кривой §Na (ф) и смещения этой КрИВОЙ При ИЗМЄНЄНИЙ Сса, НуЖНО искать на основе другой модели. Резкое возрастание проводимости обусловлено перемещением внутри мембраны заряда величины 2 ^ 4, которое должно быть связано с десорбцией одного иона Са++. Если заряд совершает в поле работу гссфЗ2", где га — 3,5, то для получения согласия с опытом надо принять близкое к нулю значение р, т. е. малую кооперативность или ее отсутствие.
Модель, объясняющая основные экспериментальные факты, предложена в работе [68].
^Са + А^В.
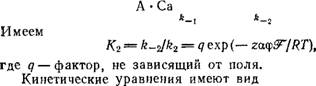
(4.58)
Допустим, что в мембране имеется N ячеек, каждая из которых содержит молекулу или группу молекул (активирующую частицу, способную находиться в состоянии[3]) А или В. Предположим, что переходы А В связаны с совершением работы в электрическом поле. Такие переходы могут состоять в перемещении заряженной молекулы, в поворотах диполей или в конформационном превращении макромолекулы, приводящем к одновременному перемещению нескольких зарядов. Последний вариант подтверждается опытами, свидетельствующими о наличии структурных изменений мембраны во время увеличения проницаемости [76, 77]. Если г — суммарный заряд, перемещаемый при переходе А—* В, то работа моля частиц равна гаср^. Предположим, что в состоянии А частица образует комплексы А • Са с ионами Са++. В состоянии В активирующая частица обладает такой структурой или положением, что способствует прохождению иона Na+ через мембрану. Перенос Na+ лимитируется числом частиц в состоянии В. Обозначим числа активирующих молекул в состояниях А и В через х к у, а число комплексов А • Са через s. Имеем
§т = кУ-
Таким образом, исследование временных изменений проводимости при сдвиге ф сводится к изучению зависимости y(t). Модели отвечает схема реакций
У = k2X — k-2y, s = k^c^x kis, x + y + s = N.
Из изложенного выше следует, что пиковой Na-проводимо- сти соответствует значение у, близкое к равновесному значению yeq. В стационарных условиях, т. е. при у = s = 0, из (4.58) получаем
Где Ki = k-i/ky. Учитывая значение /С2, получаем £ка = = ^Na, шахД1 + С1 + *>ССа) Я *ХР (- ^f-)] , (4.60)
Где gNa. max = kN (k — коэффициент пропорциональности). Как МЫ видели, экспериментальная форма кривой gNa(tp) хорошо описывается формулой такого вида, если га « 3,5. Смещение кривой (4.60) вдоль оси ф при изменении сса дается условием
(1 + KlCca)q ехр = const. (4.61)
Если К\ ссі» что согласуется с представлением о комплексах А ■ Са как о резервуаре активных частиц [68], то из (4.61) следует
1п ССа — 20^Г = const (4.62)
И величина Аф при е-кратном изменении сса равна RT/za&~, что дает 7 мВ при га — 3,5. Это хорошо согласуется с опытом [71, 73, 75]. Такие же смещения кривой £ка(ф) вызывают другие двухвалентные ионы: Mg++, Со++, Cd++, Ва++, Zn++ и Ni++. Очевидно, что они могут замещать Са++ в рассматриваемой модели.
Кривая ЈNa(<p) смещается также при изменении рН [63]. При рН < 5,5 Аф == 13,5 мВ, при рН > 5,5 Аф == 1,3 мВ при е-кратном изменении концентрации Н+. Если ионы Н+ могут попарно связываться активирующими частицами в состоянии А, то их требуется в два раза больше, чем ионов Са++. Условие смещения (4.62) приобретает вид
In (1 + /Сі [н+]2) - zaq>&-/RT = const (4.63)
И, если /Сі[Н+]2> 1, то
2 In [Н+] — zayST/RT = const. (4.64)
Увеличение [Н+] в е раз равносильно уменьшению ф на величину
Аф = 2RTlza&~ = 2RT/3,b3T = 14 мВ,
Что совпадает с опытными данными в области рН <; 5,5.
При малых [Н+], если /Сі[Н+]2<1, формула (4.63) также приводит к совпадению с опытом [68].
В нестационарных условиях решение уравнений (4.58) имеет вид
У (0 = г/о + г/і ехр (г+ у2 ехр (га/). (4,65)
Кривая, описываемая (4.65), имеет S-образную форму (рис. 4.26), что согласуется с видом экспериментальной кривой gNa (0- Константы Уі и г і зависят от параметров системы ku k-i, N, сса - Подобрав численные значения констант, можно добиться полного согласия теоретической кривой (4.60) с экспериментальной. Аналитическое исследование y(t) позволяет установить зависимость начальной скорости изменения gNa(O) от сса - Расчет дает эту начальную скорость [68]
GNa (0) = - k_x NcCaK2/( 1 + Ks). (4.66)
Опыт подтверждает линейную зависимость скорости падения gNa от Сса при снятии деполяризации. Действительно, пониже - у ниє Сса в пять раз от 112 до 22 мм умень-
Шает скорость изменения gNa также в пять f раз, а от 112 до 4,4 мм — в 25 раз. Из
/ формулы (4.66) следует также, что, ском-
/ пенсировав уменьшение Сса изменением ф
/ так, чтобы произведение /Сг^са оставалось
J постоянным, мы должны наблюдать умень-
^— шение скорости падения gNa, потому ЧТО Ki
T входит еще и в знаменатель. Рис. 4.26. График ^а же модель позволяет рассчитать
Функции y(t). влияние Сса НЭ кинетику подъема gNa при возникновении деполяризации [68]. В согласии С ОПЫТОМ теория дает замедление скорости роста gNa при увеличении сса-
Таким образом, модель объясняет большую совокупность фактов, относящихся к Na-проводимости клеточной мембраны. Можно думать, что сходный физико-химический механизм определяет и изменения К-проводимостн.
Рассмотрим теперь инактивацию Na-проводимости возбудимой мембраны.
Ходжкин и Хаксли высказали две альтернативных гипотезы о природе повышения gNa [50]. Первая из них предполагает химическое превращение активирующих частиц после их перемещения из положения, которое они занимали при потенциале покоя. Вторая предполагает, что уменьшение gNa обусловлено перемещением особых инактивирующих частиц, постепенно блокирующих каналы проводимости. Вторая гипотеза принята в теории Ходжкина — Хаксли (см. стр. 179). Модель, предложенная в работе [67], исходит из первой альтернативы.
При потенциале покоя активирующие частицы находятся преимущественно в состоянии S, когда они связаны с Са++ и А. Эти состояния отвечают отсутствию Na-проводимости. При де-
поляризации мембраны происходит переход А->В в проводящее состояние, связанный с перемещением заряда z в полеаср. Из состояния В активирующая частица может переходить в неактивное состояние С. Этот переход не связан с перемещением заряда. После снятия деполяризации происходит переход С —► S ( = А • Са) с работой заряда zaq>@~. Схема этих процессов показана на рис. 4.27. Соответствующая система кинетических уравнений имеет вид
X=k]s — k-ixc са + k-2y — k2x, у = k-3u — k3y — k-2y + k2x, й — — k-3u - f k3y + &-4s — kiUCa, x-\-y-\-и-\-s=l.
Здесь x, y,u, s — доли молекул в состояниях А, В, С, S (== А ■ Са) соответственно, сса — концентрация Са++ в омывающем растворе. Как уже сказано, gNa = ky (см. стр. 196). Исследование изменений gNa ВО времени СВОДИТСЯ к определению y(t).
Считая, что в реакции II быстро устанавливается равновесие (это согласуется с наблюдаемым ' влиянием сса на кинетику активации), заменим первое уравнение (4.67) на
Х = К2у, (4.68)
Где константа равновесия К\ = k-ijki. Константы К\ и Кз, очевидно, не связаны с перемещением зарядов в поле и не зависят от <p. К2 и К4 должны зависеть от <р согласно формулам
= Я2 ехр (— zaq>&~/RT); КА = q4 ехр {zayST/RT). (4.69) Система уравнений (4.67) приводится К ниду
6-ТТЖ7І1 - 0 + + +it) У ~ О ~ ТГ) "]• 1
(4.67)
II
Ь

Рис. 4.27. Схема процесса активации и инактивации Na-проводимости [50].
I к,
К3 пі
К4 Ж
(4.70)
Нужно найти корни г\, г2 характеристического уравнения системы
+ [тТ7с7([4] + + ССа*Л) + Л-4 ( 1 + +15:)] '+
+ ТТТ7 [О + *« + сс.*Л) (1 + W, + -
Комплексным корням соответствует переход системы в стационарное состояние в результате затухания колебаний около этого состояния. При фиксированном потенциале ионные токи не испытывают затухающих колебаний. Ищем решение (4.70) с вещественными корнями г і и г2. Они отрицательны и решение записывается следующим образом:
У (0 = аі + 6, ехр (- | п Ю + сі ехр (- | г210, и (0 = а2 + Ь2 ехр (- j г, 10 + с2 ехр (-1 г211). (4J2)
Введя начальные значения у0, и0, уо, ы0 и равновесные значения
Уоо, и», отвечающие t-+oо, получим
Л — „ А — Уо + (Уоо — Уо) Г[ — г2
С _ Уо+ /-1 (у^ — Уо)
' /"2 — г,
И аналогичные выражения для а2, с2. Функция y(t) может иметь максимум в момент времени
T* ±= - 1 In Г2 + Г] (Уа> '
Г\ — Г2 г, [г/о 4- Г2 (уж — г/о)1 '
Необходимые и достаточные условия существования максимума суть
Уо + гх {уж — уо) > 0, Уо + г2 {ух — Уо) > 0. Точка перегиба соответствует
R = 1 1п Г1 [3?о + {Уо° - Уо)] ^
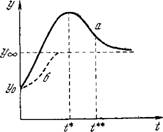
Рис. 4.28. Вычисленная зависимость у (t), т. е. gNa (/).
А —кривая при наличии максимума, б— кривая без максимума.
R{-r2 r'i [г/0 + /-2 (»» - Уо)] '
T**>i*, т. е. точка перегиба лежит вправо от максимум? (рис. 4.28). Если условия появления максимума не выполнены, то кривая имеет лишь перегиб (кривая б на рис. 4.28). Сказанное относится и к u(t). В системе уравнений (4.70) при начальных условиях уо л? «о 0 Получается г/о ~ &i/(l + К2), «о ~ 6-4.
Из опыта известно, что инактивация развивается существенно медленней, чем активация. Поэтому следует предположить, что скорости реакций III и IV (см. рис. 4.27) малы по сравнению со скоростями реакций I и II, т. е.
Ku /г_ь k2, /г_2>/г3, /г_3, /г4, /г_4. (4.73)
Поэтому г/о «о и y(t) имеет вид кривой а (см. рис. 4.28). Если бы мы отказались от принятого адиабатического приближения, то кривая y(t) имела бы второй перегиб при і < t* (кривая б на рис. 4.28, ср. рис. 4.26).
Максимальное значение у равно
— „ У о + Аг ~ Г Уо + П (У — У о) г 2 у ■/(<•!-о) Утп-Усо ^ [уо + глу^-уо) ■
(4.75)
При выполнении условий (4.73) находим из (4.71)
_ К (1 + *2 + СсаЗД) Гі~ Т+Т2 '
_ *-4*С. Уі*2 + *з. у у
Г2~ 1 + /С2+ССаК,/С2 ССаК4-й-
Следовательно, J/-i|>j/-2|, rj(ri — r2)» 1 и формула (4.74) сильно упрощается:
У max — Уо• (4.76)
Подставляя в (4.76) значение г/0 из (4.70), получаем в конечном счете
Утих == (4-77)
И в пределе но—♦■О
= 1 + (1 + сСа*і) я2 «р.(- гщПЯТ) • (4-78)
Последняя формула совпадает с (4.60). Начальное значение и0 может отличаться от 0, оно зависит от исходного состояния мембраны. Стационарное значение «о, получаемое из (4.70) при у = й = 0, равно
1 +/С3 + (1 + сСа^) К2рК3
)ане, на которой дост потенциал фр. Введ
W — и I и* =1 — «л. v ах / "ma^ q
"о = ир = . „ . , • (4.79)
К2р соответствует мембране, на которой достаточно долго сохранялся предварительный потенциал фр. Введем отношение
Его значение для стационарного и0
1 + ехр (Za<!p! r/RT)/q2 (1 + сСа/С,) К3 ' (4'80)
Эмпирическая зависимость, найденная Ходжкином и Хаксли, имеет вид
W" — TZ 7~kr,—ГП^л' (4,81)
1 +ехр (фр/7)/ехр (фр/7)
Где фр — эмпирическое значение фр, отвечающее w = 0,5 (величины фр и фр в мВ).
Как мы видели za ж 3,5, RT/&~ ж 25 мВ. Коэффициент при фр в теоретической формуле (4.80), определяющий форму кривой а>оо(фр), действительно равен za@~/RТ = 3,5/25 ж 1/7 мВ. Фактор ехр(—фр/7) в эмпирической формуле задает положение кривой а>оо(фр) относительно оси фр. Сравнивая (4.80) и (4.81), находим
Ехр(Ф;/7) = <72(1 + ссЛ)*з-
Положение кривой стационарной инактивации зависит от сса. Если Сса. Кі 1, то должно быть
CCa еХР — const.
Это значит, что е-кратное увеличение сса может быть скомпенсировано уменьшением фр на величину Дфр = RTIzatF ~ 7 мВ. Опыт дает Дфр = 6,3 — 7,8 мВ [75].
Рассмотрим теперь развитие процесса инактивации во времени. Если мембрана выдерживалась при потенциале фр недостаточно долго, то «о в выражении w = 1 — и0 зависит от длительности предварительного импульса, Uo = u(tp). При tp = 0 мембрана находится в состоянии покоя (соответствующие величины снабжаются верхним индексом нуль). Из (4.72) и значений <h, Ь2, с2 следует с учетом малости начальной скорости изменения
Й Up) = Щ> + r/lri (Up — и0) [ехр (— | г21 tp) — ^ ехр (— | п | ґр)]
(4.82)
И, так как | r21 - С | г\ |, то
И (tp) + («° — ир) ехр (— | г21 tp),
Т. е.
W « 1 — Up — (и0 — Up) ехр (— I Г2 I tp).
Мы видим, что если мембрана до подачи тестового потенциала была гиперполяризована, т. е. ир < и0, то пиковый Na-ток ра
стет экспоненциально с ростом tv\ если же ир > и° (деполяризация), то он экспоненциально убывает (рис. 4.29). Именно такой ход экспериментальных инактивационных кривых наблюдался в работе [79]. В этой работе вводится величина тд, равная в излагаемой теории |г2|-1. Расчет дает
(4.83)
(4.84)
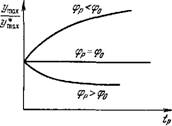
Рис. 4.29. Зависимость пикового Na-тока от длительности предварительного импульса — потенциала <рр. Фо — потенциал покоя.
. 1 КзО+^ + ССаЗД
Тй = I Г 21
Или, согласно (4.79),
K-3 + CCak4
Теория Ходжкина — Хаксли (см. стр. 177) дает
= wjx,
Где х— константа скорости выхода из инактивированного состояния. Знаменатель теоретической формулы (4.84) имеет тот же смысл. В теории Ходжкина — Хаксли зависимость параметров от tp подбирается искусственно с целью получения согласия с опытом; в излагаемой теории эта зависимость имеет непосредственное физическое содержание. Напишем (ср. (4.69))
Ki = л>4 ехр (— za(f>&~/2 RT),
/г _4 = v_4 ехр (zaqpS^/2 RT).
Как уже сказано, предполагается, что реакция смещена в сторону С, т. е. k-zlh < 1. При малых знаменатель в (4.84) приблизительно равен (ф измеряется в милливольтах)
CCa^4==CCaV4eXP(-(P/14)-
Опыт дает и = 0,07 ехр(—qp/20).
Согласно теоретической формуле (4.83) тл(ф) представляется произведением двух противоположно направленных 5-образных кривых, т. е. тл(ф) имеет колоколообразную форму. При ф—»—оо тл—>0, при ф—»оо Такую же форму имеет экспери
Ментальная кривая.
Согласно (4.83), максимум кривой та(ф) смещается в сторону больших ф с увеличением сса - Именно такое влияние Са++ на величину xh наблюдалось в работе [75].
Таким образом, описанные кинетические модели действительно дают количественное описание большой совокупности
явлений, наблюдаемых при генерации потенциала действия — при активации и инактивации мембраны. Вскрывается взаимосвязь различных явлений. Излоя-енная теория согласуется с экспериментальными фактами. Основная ее идея состоит в том, что переходы Ач=^В и S С связаны со структурными превращениями мембраны. Основной параметр теории — величина za. Опыт показывает, что при изменении проводимости мембраны аксона, при ее возбуждении, происходят структурные изменения. В работах [76, 80] наблюдались изменения рассеяния света. Тасаки и сотрудники наблюдали изменения флуоресценции [77], Берестовский и др. — изменение двулучепреломления мембраны аксона,.вызванное появлением потенциала действия [81].
Прямые доказательства перемещения заряженных частиц, входящих в структуру мембраны, под действием поля были получены впервые Армстронгом и Безанилья, а затем изучены ими и другими исследователями более подробно [82, 83, 97].
При смещении мембранного потенциала в положительную сторону наблюдается изменение проводимости, при смещении в отрицательную сторону изменения нет. Следовательно, имеются «активационные ворота» — это свойство мембран нелинейно. Для нахождения реального тока заряженных частиц необходимо, во - первых, выделить нелинейные компоненты мембранного тока, и, во-вторых, связать их с процессом активации.
Чтобы обнаружить малый компонент трансмембранного тока, необходимо исключить мощные ионные токи, основную часть которых составляют токи Na+ и К+. В цитированных работах эти ионные токи подавлялись путем замены проникающих ионов иепроникающими. Ионы Na+ в наружном растворе заменялись ионами трис (оксиметил) метиламмония, а ионы К+ — ионами Cs+. Использовался также эффект Коля и Мура [97], позволяющий существенно замедлить развитие К-тока с помощью большой предварительной гиперполяризации мембраны.
Для устранения линейных токов утечки и емкостных токов применен метод алгебраического сложения сигналов, полученных от двух скачков потенциалов, равных по величине, но противоположных по знаку. Получающиеся суммарные токи очень малы. Поэтому для улучшения соотношения «сигнал — шум» применялась техника суммирования сигналов. Суммировались и усреднялись ответы от сотен и даже тысяч пар сигналов.
Каков источник зарегистрированных таким методом токов? Армстронг и Безанилья подробно доказывают, что это не токи ионов, приходящих из раствора. Следовательно, это токи смещения зарядов, являющихся структурной частью мембраны. Кейнес и Рохас [83] приводят следующие аргументы в пользу -того, что наблюдаемые токи являются токами смещения: 1) суммарный заряд, смещенный при включении деполяризующего потенциала, с большой точностью равен суммарному заряду, смещенному при снятии деполяризации; 2) смещенный заряд, возрастая с увеличением приложенного потенциала, достигает предельной величины при достаточно больших импульсах; 3) понижение температуры не меняет полного заряда, перенесенного при прохождении импульса данной величины, хотя константа времени имеет большой температурный коэффициент.
Идентификация несимметричных токов смещения с процессами, управляющими развитием Na-токэ, требует детального и разностороннего изучения свойств этих токов. В пользу связи между обоими процессами говорит близость их временных констант (200—400 мкс). В аксонах, не дающих Na-токэ («dead axon pattern»), не наблюдаются и асимметричные токи смещения. Внутренняя перфузия ЮМ рзствором ZnCl2 обратимо подавляет Na-ток и несимметричный ток смещения. Ряд других свойств, по которым можно идентифицировать эти процессы, является в настоящее время предметом дискуссии. Требуются дальнейшие исследования, чтобы установить, каков механизм участия зарядов, дающих несимметричные токи смещения, в изменениях Na-проводимости.
Процессы, определяющие изменения Na-проводимости, изучаются также на основе исследования влияния на нее различных ионов. Выше рассмотрено влияние Са++ и Н+ (см. стр. 196). Ионообменные процессы, как уже не раз указывалось, весьма существенны для поведения мембран. Эдельман и Палти изучали влияние ионов К+ в окружающем растворе на инактивацию №+-проводимости [84]. Параметр инактивации wx убывает с ростом концентраций К+, временная постоянная тл возрастает. Эти и другие явления также удается объяснить на основе кинетической модели, учитывающей ионный обмен [70]. Модель предполагает, что центры, определяющие мембранную проводимость, могут существовать в двух состояниях. При переходе из одного состояния в другое производится работа заряда в электрическом поле. Одно из этих состояний (S) стабилизируется ионами Са++. При их замене ионами Na+ или К+ центр приобретает способность к быстрому переходу в другое состояние, что приводит к высокой Na-проводимости, если ионы Na+ связаны с этим центром. Связывание К+ переводит центр в состояние инактивиро- ванной Na-проводимости.
Сходная схема может объяснить действие других ионов на gNa, в частности, ингибирующее действие яда — тетро - дотоксина.
Кинетические модели не дают, конечно, полного молекулярного истолкования обсуждаемых явлений. Здесь необходима дальнейшая экспериментальная работа, раскрытие тонких количественных закономерностей. Но можно считать установленным.
Что в соответствии с развиваемыми представлениями о конфор- мационных свойствах мембран (см. § 3.8), их функциональные участки переходят из одних состояний в другие и эти переходы зависят от внешнего поля и ионного окружения.
Физика нервного импульса изложена также в обзоре [98].