Электронный Парамагнитный резонанс в биологии
Метод быстрого замораживания
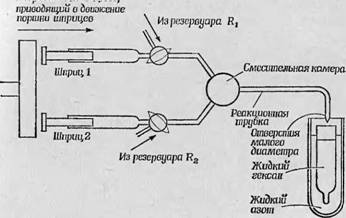
В основе метода быстрого замораживания, используемого' для изучения кинетики короткоживущих промежуточных продуктов, лежит тот же общий принцип, с тем отличием, что реакционная смесь не проходит непосредственно через резонатор, а быстро впрыскивается в какую-либо охлаждающую жидкость. Здесь смесь быстро замораживается, и тем самым фиксируется равновесная концентрация продуктов, имевшая место в момент- замораживания. Такой прибор изображен на фиг. 35. Его смесительная часть устроена так же, как и в более простом приборе, применяемом для измерений в непрерывном потоке; из смесителя реакционная смесь течет по трубке, проходит через капиллярное отверстие и мгновенно замораживается. Это устройство должно удовлетворять следующему принципиальному требованию: время замораживания должно быть мало по сравнению со временем протекания изучаемой реакции. Чтобы достигнуть этого, реакционную смесь впрыскивают в охлаждаемую жидким азотом жидкость, с которой ни один из реагентов не смешивается. Лучше даже использовать не жидкий азот, а какую-либо другую среду с более высокой температурой кипения, поскольку пузырьки газа, образующиеся в азоте, замедляют теплоотдачу реакционной смеси. Эффективность быстрого охлаждения подробно изучал Брэй [6]; он показал, что если водные растворы, находящиеся при р. ммпатпой температуре, впрыскивать через узкую трубочку и. нлметром 0,2 мм в гексан, температура которого равпа —80° С, in время замораживания не превышает 10 мс. Из этого следует, •I10 метод быстрого замораживания можно очень эффективно исполь - uiiiiiTb при изучении кинетики ферментативпых реакций или ( чодпых с ними процессов, в которых короткоживущие промену сочные продукты сохраняются в течение 50 мс и более.
|
Rudnnn. mi4Pr. Kim ППРГ. Г
Фиг. 35. Принципиальная схема прибора для измерений методом быстрого Замораживания. Объяснение см. в тексте. |
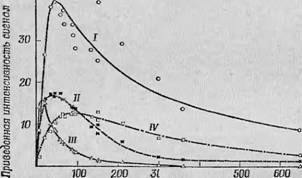
Пример исследования кинетики биохимической реакции с помощью этого метода приведен на фиг. 36, где представлены результаты, полученные в экспериментах с к с а пт и н о к с ид а з ой l7]. В этой реакции возникает высокая концентрация промежуточных нестабильных свободных радикалов и одновременно происходят три параллельных изменения валентностей в металлах переходной группы, связанных с ферментом. На фиг. 36 кинетика этих валентных изменений сопоставлена с изменением концентрации - свободных радикалов. Эти результаты хорошо иллюстрируют ценность метода ЭПР, позволяющего проводить корреляцию между активностью свободных радикалов и одновременным изменением валентности металлов в ферменте. Подробно значение этих результатов мы обсудим в гл. 5, а здесь привели их лишь потому, что они удачно иллюстрируют эффективность метода быстрого замораживания.
Чтобы этот метод дал наилучшие результаты, должны быть точно соблюдены следующие экспериментальные условия. Во-первых, скорость поступления жидкостей в смесительную камеру должна достигать установленного значения в максимально короткий срок и затем поддерживаться на этом уровне до тех пор, пока в замораживающую жидкость через выходное отверстие не попадет достаточное количество реакционной смеси. После этого поток должен быть мгновенно остановлен, чтобы объем материала, замороженного в охладительной камере, всегда соответствовал одному и тому же времени прохождения реакционной смеси через выходную трубку. Поэтому для обеспечения точности и воспроизводимости перемещения поршней следует использовать гидравлические прессы или какие-либо аналогичные
|
С 40
Фиг. 36. Полученные методом быстрого замораживания кривые, характеризующие кинетику ксаитиноксндазы [7]. Хорошо видны изменения концентраций промежуточных свободных радикалов (I) и различных ионов металлов (II и III — компоненты сигнала Mo(V), IV — Ре).ч -Л Ю 400 Время, мс |
Им устройства, так как любая допущенпая здесь ошибка непосредственно влияет на точность кииетических измерений. Охлажденный гексан (или любую другую жидкость, в которую впрыскиваются реагирующие растворы) можно поместить в сосуд с узким (около 3 мм в диаметре) отростком и собирать замороженный материал в этом отростке, чтобы затем непосредственно помещать его в резонатор ЭПР-спектрометра. Этот способ обычно используют во всех случаях, когда количество изучаемого материала ограничено. Применение низкой температуры не только позволяет проводить измерепия ничтожных количеств замороженного материала в удобное для исследователя время, но и резко повышает чувствительность самих измерепий.