Добавки в бетон Справочное пособие
МЕХАНИЗМ ГИДРАТАЦИИ
1.5.1. Трехкальциевый и двухкальциевый силикаты. Механизм гидратации индивидуальных составляющих цемента и самого цемента является предметом серьезных дискуссий и разногласий. В своей ранней теории Ле-Шателье представил гидратацию цемента через растворение безводных соединений, за которым следовало сцепление и осаждение кристаллов гидратированных соединений. Михаэлис считал, что когезия является результатом образования и последующего высушивания геля [19]. В последнее время получило развитие представление о топохи - мическом или твердофазовом механизме.
Несмотря на большое число работ в этой области, все еще остается неясным представление о механизме гидратации C3S — главной фазы цемента. Для его объяснения предлагается принять в расчет некоторые стадии, через которые проходит процесс гидратации. Можно отметить пять стадий на термокинетической кривой калориметрии в изотермических условиях (рис. 1.3). На первой стадии, как только C3S вступает в контакт с водой, наблюдается сначала скачок скорости тепловыделения, а затем ее падение в течение 15—20 мин. Эта стадия называется предындук - ционным периодом. На второй стадии скорость реакции очень низка. Это — индукционный период. Он может длиться в течение нескольких часов. В это 18 время цементное тесто сохраняет свою пластичность и удо - боукладываемость. Предполагают, что первые две стадии, на которые удается воздействовать с помощью добавок, оказывают влияние на последующую гидратацию C3S.
На третьей стадии реакция протекает активно, с самоускорением, достигая максимальной скорости к концу этой стадии. Время, отвечающее началу схватывания, приблизительно совпадает с тем временем, когда скорость реакции начинает сильно возрастать, а время до конца схватывания — с временем завершения третьей стадии.
|
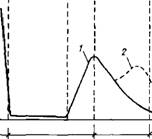
Стадия I К Ш Ш 4h------------ f----- f------------ 1
Мин ч ч сут сут Рис. 1.3. Термокинетические кривые (изменение скорости тепловыделения v во времени) для процессов гидратации C3S (1) и портландцемента (2) |
|
ЗГ |
|
£ <i) I П |
На четвертой стадии скорость тепловыделения C3S постепенно уменьшается. Продолжается гидратация C3S. На последней — пятой стадии образуется лишь небольшое количество продуктов гидратации C3S. Эта стадия контролируется процессом диффузии.
Наибольшее внимание уделяют первым двум стадиям. На первой, как только C3S входит в контакт с водой, в раствор переходят кальций - и гидроксил - ионы. На второй стадии продолжается растворение C3S, и рН растет до 12,5. Здесь образуется небольшое количество силикатов. После того как будет достигнута определенная критическая концентрация кальций - и гидроксил - ионов, начинается быстрая гидратация C3S с образованием Са(ОН)г и C-S-H (третья стадия).
Много публикаций посвящено объяснению механизма, вызывающего индукционный период и его последующее окончание. В основном считают, что начальные продукты реакции образуются на поверхности C3S, что замедляет дальнейшую реакцию. Возобновление реакции вызывается разрушением поверхностной пленки. Согласно [20], первоначально гидраты имеют высокое отношение C/S — около 3, затем оно снижается до 0,8—1,5 путем перехода ионов Са в раствор. Вторичные гидраты имеют свойства, позволяющие ионам проникать сквозь них, обеспечивая возможность прохождения быстрой реакции. Превращение первичных гидратов во вторичные происходит, очевидно, за счет процессов их зародышеобразо - вания и роста кристаллов. Хотя эта теория согласуется со многими наблюдениями, имеются и другие факты, не подтверждающие ее. Например, отношение C/S продуктов ниже, чем было указано, защитная пленка недостаточно протяженная, продукт реакции — хрупкая пленка, которая легко сходит с поверхности, и первоначальное растворение может быть или не быть конгруэнтным.
Конец индукционного периода объяснялся замедленным образованием зародышей СН. Обычно наблюдали быстрый рост кристаллов СН и переход ионов Са в раствор в конце индукционного периода. Это наводит на мысль, что осаждение СН связано с началом стадии ускорения. Если осаждение СН дает толчок реакции, то добавление Са - ионов должно ее ускорять, если не происходит отравления зародышей.
Как известно, добавление извести замедляет реакцию. Образование C-S-H также не объясняет периода ускорения. В работе [21] отмечено, что дзета - потенциал гидратирующегося C3S положителен; - это может свидетельствовать о возможности хемосорбции ионов Са на образующейся поверхности C3S, а пленка является барьером между C3S и водой. Считают, что во время осаждения Са (ОН) 2 из раствора переходит Са2+ (что должно, в свою очередь, инициировать удаление Са2+ из барьера). В результате реакция гидратации ускоряется.
Другие авторы говорят о механизмах, основанных на задержке образования зародышей кристаллизации C-S-H для объяснения конца индукционного периода. Один из них предполагает, что стабилизирующее действие на C3S тонкой пленки воды заканчивается, когда высокая концентрация Са24" в растворе вызывает осаждение зародышей C-S-H.
Согласно работе [22], продолжительность индукционного периода контролирует диффузия воды через зерна C3S. Дефекты увеличивают диффузию и, таким образом, вызывают кристаллизацию C-S-H; согласно [23], хемосорбция НгО и растворение некоторого количества C3S проходят во время индукционного периода. Авторы отмечают, что конец индукционного периода связан с ростом зародышей C-S-H до критического размера.
Существуют другие представления, на первый взгляд независимые, но имеющие много общих черт [24], в которых делается попытка объяснить результаты проведенных наблюдений. Гидратация C2S протекает тем же путем, что и C3S, но значительно медленнее. Количество тепла, выделяемое C2S, много ниже, чем C3S. Кривая скорости тепловыделения не имеет таких явно выраженных пиков, как на рис. 1.3. Ускорители повышают скорость реакции C2S — Н20. Взаимодействие с водой C2S изучено меньше, чем C3S.
1.5.2. Трехкальциевый алюминат (или C4AF)+гипс + + вода. На изотермической калориметрической кривой процесса гидратации смеси СзА и гипса также наблюдаются пики (см. рис. 1.3), однако время 20 их появления и протяженность отличаются от приведенных для C3S. Согласно распространенному мнению, замедление гидратации С3А в присутствии гипса объясняется образованием тонких кристаллов эттрин - гита на его поверхности. Эта плотная пленка в индукционном периоде разрушается и вновь формируется в течение этого периода. Когда весь сульфат связывается, эттрингит реагирует с СзА, образуя моносульфатную форму гидросульфоалюмината. Это превращение происходит при гидратации цемента между 12—36 ч с одним экзотермическим пиком. Некоторые добавки могут ускорить или замедлить это превращение.
Высказывалось также мнение [25, 26], что эттрингит сам по себе не может оказывать влияние на индукционный период и что адсорбция сульфат - ионов на положительно заряженном С3А замедляет гидратацию. Предполагалось также, что осмотическое давление может воздействовать на разрыв иголок эттрингита. Это предположение базируется на факте обнаружения пустотелых иголок в системе С3А — гипс — НгО. Разрывы эттрингита приводят к перемещению ионов А1 в водную фазу с быстрым образованием пустотелых игл, через которые может быть перенесено большое количество А13+ - ионов [24].
В такой же последовательности, как и СзА, гидратирует - ся C4AF. Гипс замедляет гидратацию C4AF более эффективно, чем СзА. Однако цемейты с высоким содержанием С3А нестойки при воздействии сульфатов, а с высоким содержанием C4AF устойчивы. В высокоалю- моферритных цементах эттрингит не может образовываться из низкосульфатного сульфо - алюмината, возможно, вследствие содержания железа в мо- носульфоалюминате. Видимо, аморфный AF3 предотвращает такие реакции. Возможно также, что образующаяся суль - фоалюминатная фаза гидрати - руется таким образом, что это не вызывает кристаллизационного давления.
1.5.3. Портландцемент. Описанный выше механизм для чистых компонентов цемента является основой изучения гидратации портландцемента. Калориметрические кривые C3S и портландцемента схожи, но у портландцемента может возникнуть третий пик вследствие образования гидрата моносуль - фоалюмината (см. рис. 1.3). Детально воздействие С3А и C4AF на гидратацию C3S и C2S окончательно не изучено. Были представлены модели защитного слоя, учитывающие возможность взаимодействия [24]. Хотя начальные стадии процесса не ясны для C3S (в цементе), можно допустить, что продукты гидратации С3А образуются как через раствор, так и топохимическим путем[1].